- Introduzione: la crescente digitalizzazione nella ricerca clinica e nella prevenzione
La ricerca clinica sta subendo una trasformazione digitale significativa: tecnologie come dispositivi indossabili, smartphone con relative app e sensori remoti stanno rivoluzionando il modo in cui vengono raccolti i dati dei pazienti, migliorando la quantità e qualità delle informazioni e riducendo l’impatto sulle normali attività dei pazienti. Al centro di questa rivoluzione c’è la Digital Evidence, ovvero l’insieme di prove generate da strumenti digitali per supportare decisioni cliniche e regolatorie.
Questa evoluzione porta con sé nuove opportunità, ma anche sfide legate alla standardizzazione, validazione e accettazione regolatoria. Tra i protagonisti di questo cambiamento troviamo i Digital Endpoints, variabili misurate in continuo che stanno ridefinendo il modo in cui studiamo le malattie e valutiamo i trattamenti.
Dal punto di vista del paziente, la possibilità di essere seguito nel suo percorso clinico senza dover necessariamente recarsi in un ospedale è una opportunità generalmente molto apprezzata. Dal punto di vista della azienda farmaceutica, l’approccio al clinical trial parzialmente decentralizzato è interessante in quanto permette di raggiungere e coinvolgere una popolazione maggiore. La possibilità di raccogliere dati distribuiti in continuità nel tempo, attraverso misurazioni ripetute a intervalli frequenti e regolari (dati longitudinali) permette al ricercatore di analizzare l’evoluzione di uno stato di salute o di una patologia, invece di avere solo una serie di “fotografie” statiche nei momenti della visita. Come vedremo in seguito, questi dati longitudinali sono la vera rivoluzione della ricerca clinica.
I dispositivi digitali hanno anche un ruolo fondamentale nella cura e nella prevenzione in numerosi ambiti terapeutici. Un esempio illuminante è illustrato in un recente articolo di Chen et al. 1, che si focalizza sulle importanti sfide sociali e sulla crescente pressione sui sistemi sanitari correlate all’aumento dell’aspettativa di vita. In questo ambito, le tecnologie digitali offrono un enorme potenziale per passare dalle routine mediche tradizionali alla medicina a distanza, trasformare la nostra capacità di gestire la salute e l’indipendenza nelle popolazioni che invecchiano, e aiutare gli anziani a monitorare la propria salute e mantenere l’indipendenza a casa.
- Cosa sono i Digital Endpoints?
Un Digital Endpoint è un outcome clinico misurato tramite tecnologie digitali: parametri misurabili rilevati attraverso strumenti digitali, che sostituiscono o affiancano gli endpoint tradizionali negli studi clinici. I Digital Endpoint possono includere metriche di attività fisica, qualità del sonno, parametri cardiaci, capacità respiratoria e altri parametri rilevanti per specifiche patologie. La Digital Evidence (o “evidenza digitale”) è un concetto più ampio: si riferisce a qualsiasi dato digitale che possa supportare decisioni cliniche, regolatorie o di sviluppo di farmaci. Può includere Digital Endpoints, ma anche altri tipi di dati generati da dispositivi digitali, database sanitari, real-world data, ecc. .
A differenza degli endpoint tradizionali, rilevati durante visite in ospedale (es. una misurazione della pressione arteriosa), i Digital Endpoints catturano dati in tempo reale nella vita quotidiana dei pazienti. Pensiamo ad esempio ad un braccialetto che monitora i passi di un paziente con sclerosi multipla per valutare la mobilità, o a un’app che registra la qualità del sonno in un trial su disturbi neurologici. La differenza sta nella continuità: mentre una visita in clinica offre una misura puntuale – come una fotografia – i dispositivi digitali producono l’equivalente di un film, con migliaia di dati raccolti nel tempo, anche più volte al secondo. Questo approccio permette di osservare le condizioni di salute e l’evoluzione di una malattia con un dettaglio senza precedenti, superando i limiti delle misurazioni episodiche.
Definizione EMA: Un Digital Endpoint (una variabile precisamente definita, destinata a riflettere un outcome di interesse e analizzata statisticamente per rispondere a una specifica domanda di ricerca) è derivato da o include una misurazione digitale.
I Digital Endpoints possono essere:
- valutazioni degli outcome clinici (Clinical Outcome Assessments – COAs), il cui valore clinico viene stabilito de novo
- biomarcatori (biomarkers), per i quali è possibile stabilire una relazione affidabile con un outcome clinico esistente.
- Il passaggio da Clinical Endpoint a Digital Endpoint: esempio
Per chiarire la transizione da Endpoint Clinico a Endpoint Digitale consideriamo un esempio relativo ai trial clinici nell’ area terapeutica dell’Ipertensione Polmonare Arteriosa, per i quali l’endpoint tradizionale è basato sul Six Minutes Walk Test (6MWT): al paziente viene chiesto di camminare per 6 minuti in un ambiente ospedaliero ed un operatore osserva l’esercizio e misura la distanza percorsa.
La misura viene ripetuta ad intervalli prefissati (ad esempio ogni due mesi) ed il cambiamento tra la misura al termine del trial (ad esempio al mese 6) e la misura al baseline viene usata come endpoint. Si nota subito che l’approccio appena descritto, ancorché usato in numerosi trial clinici ed accettato dalle autorità regolatorie, presenta indubbiamente alcuni punti di debolezza: la misura è episodica, programmata ed effettuata in un ambiente diverso da quelli della vita quotidiana del paziente.
Tutti questi fattori possono influire sull’esito del test: in modo negativo (il paziente quel giorno non si sentiva bene o soffriva di ansia da prestazione, il viaggio verso l’ospedale lo ha affaticato) oppure in modo positivo (il paziente si impegna notevolmente per dimostrare a sé stesso e al medico che la terapia sta funzionando).
Questi punti di debolezza sono risolti, o comunque attenuati, passando ad una misura digitale in continuo, ottenuta con un dispositivo digitale basato su accelerometri e altri sensori. Il dispositivo, sotto forma di smart watch o smart ring, traduce le accelerazioni misurate dagli accelerometri (raw data, o dati grezzi) in misure dell’attività fisica del paziente come numero di passi, intensità dell’attività e altro (i dati derivati). I dati digitali (grezzi e/o derivati) dei partecipanti al trial clinico vengono trasmessi in automatico ad una apposita piattaforma centralizzata che permette sia allo sponsor che al medico di analizzarli e di monitorare i pazienti, e sono utilizzati per calcolare il Digital Endpoint, che a questo punto sarebbe in qualche modo simile all’endpoint clinico originario, ma basato su una quantità di dati superiore di molti ordini di grandezza .
In realtà ci si può spingere oltre, utilizzando lo stesso dispositivo per raccogliere la misura di altri parametri vitali del paziente, come HR (frequenza cardiaca) e HRV (variabilità della frequenza cardiaca), SpO2, temperatura corporea, ECG e altri: paragonando questi dati con quelli raccolti nell’approccio tradizionale si nota l’importante salto di qualità e quantità che spiega il crescente interesse per i Digital Endpoint.
Chi volesse avere una visione dettagliata dei numerosi endpoint già codificati può accedere alla “Library of Digital Endpoints” 2 curata da “Digital Health Measurement Collaborative Community (DATAcc) by the Digital Medicine Society (DiMe)”, che è una raccolta specificamente focalizzata su studi sponsorizzati dall’industria su nuovi prodotti medici o applicazioni. Si tratta di una risorsa che viene continuamente aggiornata, concepita sia come risorsa di riferimento sia come un elenco che la comunità contribuisce a costruire e mantenere. Essa misura i progressi nel campo e mette in evidenza il lavoro che viene fatto per promuovere l’uso di endpoint digitali per accelerare lo sviluppo di nuove cure.
- Finalità, benefici e sfide dei Digital Endpoints
I Digital Endpoints nascono per rispondere a una domanda cruciale: come possiamo comprendere meglio le malattie osservando i pazienti nel loro ambiente naturale? La loro finalità è duplice: migliorare la conoscenza delle patologie e fornire evidenze robuste per le autorità regolatorie, come EMA e FDA. I benefici includono: maggiore precisione e sensibilità nella rilevazione di outcome clinici, possibilità di raccogliere dati in tempo reale e in ambienti reali (real-world evidence) e riduzione del carico per i pazienti e miglioramento dell’aderenza agli studi. Non mancano ovviamente le sfide:
- Validazione analitica e clinica degli strumenti digitali: come possiamo essere sicuri che le misure ottenute (ad esempio il numero di passi compiuti durante il giorno) sono corretti per tutte le categorie della popolazione interessata, indipendentemente da genere, età, peso, altezza ed etnia? E come dimostrare che la misura ottenuta (ad esempio i passi) riflette davvero lo stato di salute del paziente?
- Accettazione regolatoria e integrazione nei processi decisionali delle autorità sanitarie
- Standardizzazione dei dati e interoperabilità tra sistemi
- Il digital divide: non tutti i pazienti sanno usare smartphone o wearable
- La privacy: i dati raccolti in continuo devono essere protetti da violazioni.
Tuttavia, queste sfide non sono insormontabili: collaborazioni tra industria, accademia ed enti regolatori stanno tracciando la strada.
- Approfondimento dei benefici dei Digital Endpoints
Uno studio recente 3 ha analizzato dati dalla Biblioteca degli Endpoint Digitali della Digital Medicine Society (DiMe) e dal registro degli studi clinici statunitense, ClinicalTrials.gov. Sono stati considerati più di 10.000 studi clinici appartenenti a 3 aree terapeutiche: cardiovascolare, sistema nervoso centrale e diabete. I dati mostrano chiaramente che i Digital Endpoints permettono di ridurre il numero di pazienti arruolati e la durata dello studio.
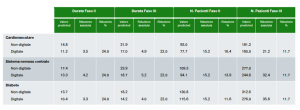
Tabella 1. Impatto dell’utilizzo di Digital Endpoints su durata e sample size di studi clinici. Durata degli studi espressa in mesi. Modificata da DiMasi et al. 3
Sulla base dei dati è stato sviluppato un modello di valore netto attualizzato atteso (eNPV) dei flussi di cassa per lo sviluppo e la commercializzazione di nuovi farmaci e calcolato il ritorno sull’investimento (ROI) come rapporto tra l’incremento stimato nell’eNPV e il costo medio di implementazione degli endpoint digitali.
Per gli studi di fase II, l’aumento dell’eNPV variava da 2,2 milioni a 3,3 milioni di dollari, con ROI tra il 32% e il 48% per indicazione. I benefici netti erano sostanzialmente più elevati per gli studi di fase III, con l’aumento dell’eNPV che variava da 27 milioni a 40 milioni di dollari, con ROI da quattro a sei volte l’investimento. Questo studio dimostra che, nonostante la necessità di un investimento iniziale sostanziale, gli endpoint digitali stanno generando un notevole eNPV (valore netto attualizzato economico) e ROI (ritorno sull’investimento) per l’industria dello sviluppo farmacologico.
Gli endpoint digitali non si limitano a promettere di affrontare alcune delle maggiori sfide che la ricerca clinica di oggi deve affrontare, ma stanno attivamente catturando questo valore già oggi.
- Il percorso di verifica e validazione
Come accennato in precedenza, gli strumenti su cui si basano i Digital Endpoints devono superare diverse fasi di verifica e di validazione. Un primo framework 4, sviluppato nel 2020 e denominato V3 (Verification, Analytical Validation, Clinical Validation), richiedeva la verifica tecnica, la validazione analitica e la validazione clinica. L’esperienza maturata negli anni seguenti e l’osservazione di inconvenienti, come errori o dati mancanti, ha portato allo sviluppo di un modello aggiornato 5, denominato V3+, che richiede l’aggiunta dalla Usability Validation.

Tabella 2. Il percorso di verifica e validazione di Digital Endpoints 4,5
- Il prossimo passo: accelerare e ottimizzare l’adozione della Digital Evidence e dei Digital Endpoints
Come in tutte le fasi di radicale cambiamento, anche in questo caso la transizione richiede capacità, organizzazione e impegno da parte di tutti gli attori del sistema: aziende farmaceutiche, ricercatori, enti regolatori, aziende tecnologiche e associazioni di pazienti costituiscono un ecosistema complesso e molto interconnesso.
Se ogni progetto viene affrontato in modo competitivo e se ogni singolo componente del sistema affronta il cambiamento in autonomia, la transizione andrà incontro a tempi lunghi e al rischio di spreco di risorse; per evitare questa eventualità sono nate società e gruppi di lavoro che propongono un approccio collaborativo, basato sulla condivisione pre-competitiva, sulla standardizzazione e armonizzazione delle misure digitali e dei processi che ne guidano la scelta, la validazione e l’implementazione.
Un esempio concreto in questo senso è DEEP (Digital Evidence Ecosystem and Protocols, www.deepmeasures.health). Questa iniziativa, nata dalla collaborazione tra industria ed enti regolatori, mira a standardizzare lo sviluppo dei Digital Endpoints, basandolo su un modello condiviso e standardizzato. Ponendosi come obiettivo finale quello di migliorare la salute umana, e constatando che le tecnologie di salute digitale sono ancora sottoutilizzate in questo ambito, che sviluppare misure digitali incentrate sul paziente è complesso e costoso, DEEP mira a connettere, non a competere. DEEP collabora con l’industria farmaceutica, aziende tecnologiche, fornitori di servizi specializzati, autorità sanitarie, enti accademici e gruppi di pazienti per promuovere lo sviluppo e l’adozione di misure digitali da utilizzare negli studi clinici.
- Conclusioni e invito all’azione
I Digital Endpoints e la Digital Evidence sono una opportunità per la ricerca clinica, la prevenzione e la cura. Le sfide tecniche e regolatorie esistono, ma il loro superamento è alla portata, grazie a iniziative come DiME e DEEP.
Aziende farmaceutiche e Clinical Research Organizations possono fare la differenza: investendo in soluzioni digitali e partecipando a progetti collaborativi, contribuiranno a plasmare questa rivoluzione. La ricerca clinica non è mai stata così vicina al mondo reale: sta a noi coglierne le opportunità.
Massimo Raineri 1, Gualberto Gussoni 2, Sergio Scaccabarozzi 3
1 Business Partner Consulting Clinical, Arithmos Srl
2 Presidente, Fondazione RIDE2Med
3 Vice-Presidente, Fondazione RIDE2Med
Bibliografia
- Chen C, Ding S, Wang, J. Digital health for aging populations. Nat Med 2023; 29: 1623–1630
- https://dimesociety.org/library-of-digital-endpoints/
- DiMasi JA, Dirks A, Smith Z et al. Assessing the net financial benefits of employing digital endpoints in clinical trials,. Clin Transl Sci 2024; 17: e13902
- Goldsack JC, Coravos A, Bakker JP. Verification, analytical validation, and clinical validation (V3): the foundation of determining fit-for-purpose for Biometric Monitoring Technologies (BioMeTs). npj Digital Medicine 2020; 3: 55
- Bakker JP, Barge R, Centra J et al. V3+: An extension to the V3 framework to ensure user-centricity and scalability of sensor-based digital health technologies Preprint https://datacc.dimesociety.org/wp-content/uploads/2024/02/V3_

