Lo scorso 11 settembre si è tenuto il webinar “Aree grigie nei Source Documents”, organizzato da SIMEF, che ha registrato un’ampia partecipazione.
L’evento formativo, promosso dal gruppo RICMA (Ricerca Clinica & Medical Affairs) in collaborazione con i colleghi e gli amici di GIQAR e GIDMcrc, è nato dall’esigenza di confrontarsi ed approfondire le nuove prospettive di gestione della documentazione e dei Source Records (SR) nell’ambito della ricerca clinica alla luce delle recenti linee guida GCP R3.
In un contesto di transizione e di forte innovazione tecnologica, in cui la ricerca clinica è sempre più permeata da processi di digitalizzazione, è fondamentale che tutti gli attori coinvolti, dai centri clinici sperimentali ai promotori, fino alle CRO, si adeguino ai requisiti normativi e di qualità richiesti dalle nuove disposizioni e dalle agenzie regolatorie, individuando soluzioni efficaci per la minimizzazione dei rischi e il controllo dei processi.
All’interno di questo scenario, il webinar ha approfondito i temi di maggiore attualità e criticità nella gestione dei dati clinici, favorendo un confronto costruttivo e multidisciplinare tra i diversi attori, con ampio spazio per la condivisione di idee ed esperienze tra esperti e colleghi.
È importante sottolineare che le indicazioni e i suggerimenti emersi durante l’incontro derivano dall’esperienza diretta degli organizzatori che non intendono in alcun modo sostituirsi a quelle fornite dalle autorità regolatorie. L’obiettivo rimane quello di proporre approcci pragmatici per una gestione efficace dei Source Records e della documentazione negli studi clinici.
Cosa sono i SD
(Loretta Aureli – Francesca Vaccari)
I record originali nella ricerca clinica (“source records”) sono i documenti originali, dati e metadati, o le copie certificate dei documenti originali in cui vengono registrati per la prima volta, i dati di uno studio clinico, come la storia medica, i risultati di laboratorio e le note sui progressi del paziente.
La revisione (R3) alle GCP hao modificato il termine da “documents” a “records” per attribuirgli un significato di “neutralità del mezzo di registrazione” (media neutrality), riconoscendo esplicitamente e marcatamente che i dati originali possono essere registrati e conservati sia in formato cartaceo che elettronico.
Questi documenti devono rispettare i principi ALCOAC+, ovvero devono essere attribuibili, leggibili, contemporanei, originali, accurati e completi, oltre che disponibili, consistenti e durevoli nel tempo.
Come identificare i SD
(Chiara Povesi – Paola Trogu)
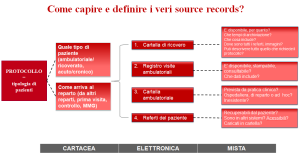
Punto di partenza per una gestione appropriata dei source record è la loro corretta identificazione. Essenziale capire quale popolazione andremo a valutare nel nostro studio e il percorso che effettueranno i partecipanti allo studio, oltre ai dati che verranno raccolti partendo dal protocollo e dalla Flowchart. Ma il vero elemento chiave per questa indagine sono le domande da porsi: a questo proposito vengono suggeriti due diversi diagrammi di flusso che, con domande dettagliate per ciascun tipo di record, guidano alla corretta identificazione dei source records. Nella maggior parte dei casi, questa analisi permetterà di identificare source record già esistenti senza la necessità di creare source records “ad hoc” per la sperimentazione.
E’ importante effettuare questa analisi prima dell’inizio dello studio, come indicato dalle GCP, per poter mettere in atto eventuali azioni mitigatrici come il coinvolgimento dell’IT (Information Technology Office) per garantire i requisiti necessari delle cartelle elettroniche, o la creazione di SOP che regolano la gestione delle cartelle ambulatoriali o il coinvolgimento della direzione sanitaria/scientifica per l’ufficializzazione delle cartelle proposte.

Quali strumenti: SD checklist – modulo ESRA
(Loretta Aureli – Francesca Vaccari)
Una corretta documentazione dei Source Records è fondamentale per garantire la conformità dei dati, dei sistemi e dei processi alle ICH GCP E6(R3). Le nuove linee guida pongono grande enfasi sulla capacità di tracciare, identificare e archiviare la documentazione clinica in modo rigoroso, assicurando integrità, trasparenza e qualità dei dati. Durante il webinar sono stati presentati strumenti pratici come il modulo eSRA (eSource Readiness Assessment) e la SD checklist, proposti come esempi di riferimenti da cui partire per strutturare i propri approcci.
- Il modulo eSRA, sviluppato dal eClinical Forum, offre uno spunto per valutare l’idoneità dei sistemi elettronici di raccolta dati, a disposizione per supportare sponsor, Fornitori di Servizi e centri clinici nel verificare se i dati generati sono adatti come fonte primaria.
- SD checklist facilita l’identificazione e la classificazione dei diversi tipi di source records (cartacei, elettronici, copie certificate), migliorandone la tracciabilità e la conformità alle normative. L’obiettivo è stato fornire strumenti flessibili e adattabili, che possono essere personalizzati per garantire qualità, trasparenza e sicurezza dei dati, in linea con le linee guida ICH GCP E6(R3).
(link al modulo eSRA: https://eclinicalforum.org/site-system-assessments/esra-handbook-and-assessment-forms-v20253 )
Validazione degli eSD o GCP compliance
(Celeste Cagnazzo – Rosita Cenna – Maurizio Polignano )
Durante la sessione è stato approfondito un tema cruciale per la ricerca clinica: la differenza tra validazione dei sistemi elettronici e reale compliance alle Good Clinical Practice (GCP) R3.
È stato chiarito come la semplice certificazione o la classe di appartenenza di un software non siano sufficienti a garantirne l’aderenza alle GCP, che si fonda invece sui principi ALCOAC+.
Sono state illustrate le principali differenze tra sistemi aperti e chiusi, con i relativi requisiti dei processi di accesso in riferimento al Regolamento eIDAS per la firma elettronica.
È emerso come la verifica della compliance richieda un’attività documentata che verifichi in maniera rigorosa la gestione degli accessi, la presenza e funzionalità degli audit trail e la protezione e tracciabilità dei dati lungo tutto il ciclo di vita del software. Infine, è stato discusso il ruolo di sponsor e centri clinici nella validazione, sottolineando l’importanza della creazione di gruppi multidisciplinari di esperti e di un approccio proporzionato al rischio per garantire integrità, sicurezza e affidabilità dei dati clinici.
Copie conformi: quando, come e perché
(Veronica Crippa – Chiara Gussetti – Stefano Stabile)
Le GCP R3 ribadiscono il concetto di copie certificate (o conformi all’originale), definite come documenti identici all’originale, in grado di preservare integralmente le informazioni contenute nel documento sorgente (inclusi layout, struttura, metadati, audit trail) e prodotti attraverso un processo verificato e validato, che può comprendere l’apposizione di data e firma del responsabile della generazione.
Tali copie certificate possono essere prodotte indipendentemente dal supporto originario del documento, sia esso cartaceo o elettronico, e, in determinati casi (quando la presenza dell’Essential Record non ha valore legale), possono persino sostituirsi all’originale.
È emerso inoltre che molti centri sperimentali che utilizzano Cartelle Cliniche Elettroniche, non potendo garantire l’accesso diretto ai propri Source Records a monitor, auditor o ispettori, ricorrono all’uso di copie certificate cartacee per le attività di verifica.
In questi casi, pur essendo chiaro l’obbligo di assicurare l’accesso diretto ai Source Records, è consigliabile implementare azioni di mitigazione del rischio, quali:
- la definizione di SOP interne per la generazione e gestione delle copie verificate cartacee,
- la redazione di un Source Data Identification Log specifico per il centro clinico,
- l’adozione di un sistema di controllo e verifica dei Source Records da parte del monitor, in affiancamento allo study coordinator (spot check).
Tali misure sono fondamentali per garantire che nessun dato venga escluso dalla verifica e dal controllo da parte del monitor, preservando così l’integrità e la qualità della documentazione clinica.
Monitoraggio dei metadati
(Selene Albiero – Rosita Cenna – Francesco Di Monaco – Francesca Vaccari)
Se i Source Records rappresentano la superficie visibile dell’informazione, i metadati ne costituiscono la trama sottostante. È proprio con i metadati che i dati clinici vengono descritti, contestualizzati e resi comprensibili, e di conseguenza interpretati e gestiti correttamente. Essi rivestono un ruolo centrale nella gestione e nell’integrità dei dati clinici, come sottolineato dalla nuova revisione ICH GCP E6(R3).
Nel contesto clinico, sono fondamentali per garantire integrità, tracciabilità e accuratezza dei dati raccolti, in linea con i principi ALCOAC+. Questi principi assicurano che ogni dato sia completo, verificabile e affidabile, consentendo una ricostruzione precisa degli eventi e delle procedure.
La E6(R3) introduce un approccio moderno alla qualità, enfatizzando la data governance e l’importanza di un approccio “fit for purpose”, ovvero adeguata agli obiettivi dello studio e proporzionata ai rischi, anche nell’ambito della gestione dei dati e dei relativi metadati. Durante il webinar sono stati illustrati esempi di metadati nei trial clinici, , come le informazioni di calibrazione di un dispositivo, la versione del software, informazioni inerenti ad un’immagini di risonanza
Al fine di approfondire l’importanza di un’adeguata attenzione ai metadati, sono stati riportati ulteriori esempi, provenienti direttamente dall’esperienza di ciascuno. Il monitoraggio dei metadati è essenziale per assicurare la qualità dei risultati, la sicurezza dei partecipanti e la conformità alle nuove normative internazionali, rendendo la ricerca clinica più trasparente, efficiente e affidabile.
Conclusioni
Il webinar “Aree grigie nei Source Documents” ha rappresentato un importante momento di confronto e aggiornamento per tutti i professionisti della ricerca clinica, evidenziando come la corretta gestione dei Source Records sia oggi uno degli elementi cardine per garantire qualità, integrità e conformità dei dati.
Le nuove linee guida ICH GCP E6(R3) impongono un cambio di prospettiva, orientato alla “media neutrality” e a un approccio basato sul rischio e sulla qualità, che richiede una collaborazione sempre più stretta tra sponsor, CRO e centri clinici.
Dall’incontro è emersa la necessità di adottare strumenti operativi concreti, procedure chiare e una solida cultura della data governance, per affrontare in modo efficace le sfide legate alla digitalizzazione e alla complessità dei sistemi elettronici.
In definitiva, le aree grigie diventano un’opportunità di crescita: uno spazio di riflessione e miglioramento continuo, in cui l’esperienza condivisa e il dialogo tra professionisti contribuiscono a costruire una ricerca clinica più robusta, trasparente e orientata alla tutela del paziente ed alla qualità dei dati.

